 / Отделка кож / Глава 1 / Оценка качества красителей / Отделка кож / Глава 1 / Оценка качества красителей
|
|
|
Изучение свойств растворов красителей в процессе крашения способствует разработке рациональной технологии крашения. Процесс крашения является весьма сложным и зависит от ряда факторов: кислотности среды, наличия в системе электролитов, концентрации красителя, температуры раствора, степени механического воздействия на окрашиваемый материал.
Водорастворимые красители обычно состоят не из отдельных ионов или молекул, а из агрегатов, в которые входит значительное число молекул или ионов. Из наиболее точных методов определения в водных растворах количества ионов красителя и агрегированных частиц необходимо отметить методы определения осмотического давления, удельной электропроводности, числа переноса, диффузии поглощения света. Несмотря на тщательное изучение свойств водных растворов красителей, до сих пор состояние красителя в растворе не может считаться окончательно выясненным.
На основании данных одних исследователей можно считать, что в растворе водорастворимые красители находятся в основном в агрегированном состоянии. Также установлено, что агрегаты красителя адсорбируют противоионы или содержат недиссоциированные молекулы.
По данным других исследователей, красители в растворах диссоциированы и их ионы могут соединяться при этом в более или менее крупные агрегаты.
Состояние красителей в растворе можно изобразить в виде трех схем, где А и К - соответственно анион и катион [1]:
|
| |
Схема I |
Схема II |
Схема III |
| Катионные красители |
К |
(nК) |
т (КА)nК |
|
| Анионные красители |
А |
(nА) |
т (АК)nА |
|
|
Схема I изображает полную диссоциацию красителя на ионы, схема II - ассоциацию ионов красителя, схема III - агрегирование частиц, включающих молекулы.
Исходя из схемы III, водный раствор красителя можно рассматривать как полидисперсную систему. При этом считается, что частицы красителя различных размеров находятся в состоянии динамического равновесия: по мере поглощения субстратом более мелких частиц более крупные распадаются и в растворе остаются агрегированные частицы различных разменов. С разбавлением раствора агрегация красителя в нем уменьшается, но новое распределение частиц по размерам происходит очень быстро.
По данным ряда авторов, агрегирование красителя в растворе происходит за счет образования водородных связей между молекулами красителя. Такое взаимодействие сопровождается выделением тепла. С повышением температуры раствора процессу агрегации начинает препятствовать тепловая энергия, подводимая извне, поэтому в таких условиях агрегирование красителя происходит медленнее, чем при более низкой температуре. Кроме того, наблюдается резкое уменьшение ассоциации молекул красителя вследствие разрушения гидратной оболочки, а также увеличение броуновского движения растворенных и диспергированных частиц, сопровождаемое разрушением агрегированных частиц. Эксперименты показали, что агрегаты прямых красителей особенно сильно изменяются в присутствии электролитов. Например, чисто-голубой при содержании хлорида натрия 1 моль/л и температуре раствора 60°С имеет число агрегации n = 24, а при температуре 97°С n=10. Из этого следует, что в растворе при температуре 97°С величина частиц значительной части красителя в 2,5 раза меньше, чем при температуре 60°С. Однако при температуре 970С и концентрации хлорида натрия, равной 2 моль/л, степень агрегации красителя увеличивается до n=29. Практически крашение кожи хромового дубления после нейтрализации и промывки ведется в красильном растворе со значительной концентрацией электролитов, что оказывает влияние на агрегирование красителя.
|
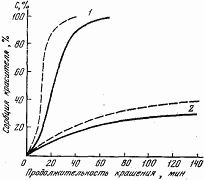
Рис.1. Влияние агрегирования красителя на его сорбцию кожей во времени при
температуре 40 0С (сплошные линии) и 60 0С (пунктирные линии):
1 -слабо агрегированный краситель; 2 -сильно агрегированный краситель
|
Следовательно, при крашении кожи часть красителя находится в виде агрегированных частиц.
Точно неизвестно, какова величина этих частиц, так как подобных исследований при условиях, близких к условиям крашения кожи, не производилось, но имеются данные о сорбировании красителя кожей при различной степени его агрегирования и разных температурах. Эксперименты свидетельствуют о значительном влиянии агрегирования красителя на его сорбцию из раствора кожей хромового дубления (рис. 1). Например, сорбирование слабо агрегированного кислотного красного при температуре 60°С в течение 25 мин достигает почти 100%, а сильно агрегированного при той же температуре за 140 мин составляет только 40 %. Резкое уменьшение сорбции красителя кожей хромового дубления может быть объяснено взаимным насыщением связей красителя в агрегированной частице.
При крашении в производственных условиях краситель находится в растворе в основном в виде ионов и частично в недиссоциированном состоянии. Большинство водорастворимых красителей в растворе ионизировано, поэтому их активность, т. е. способность сорбироваться волокном, может быть выражена как произведение активности ионов или (наиболее полно) как разность величин химического потенциала красителя в его стандартном состоянии в растворе uр и на волокне uв. Опыт показывает, что чем больше разность (uр - uв), тем полнее сорбирование красителя волокном.
В реальных условиях активность красителя в растворе может быть представлена в виде произведения Сf, где С- концентрация красителя в растворе, а f - коэффициент активности. Обычно коэффициент активности красителей приравнивают к единице. Тогда химический потенциал красителя в растворе может быть выражен формулой
|

|
где R - газовая постоянная; T - абсолютная температура раствора; С - концентрация красителя в растворе; f - коэффициент активности красителя.
Экспериментально установлено, что любое увеличение активности иона Na+, например вследствие введения в красильный раствор хлорида натрия, приводит к увеличению химического потенциала красителя в растворе. При этом, если красильный раствор находится в равновесии с волокном, то его химический потенциал на волокне увеличивается, что выражается в увеличении количества красителя, адсорбированного волокном. Во многих случаях обнаруживается, что добавление иона к любому раствору ионизированного красителя, находящегося в равновесии с волокном, приводит независимо от природы волокна к увеличению сорбции им красителя. Наиболее часто мы сталкиваемся на практике с добавлением в красильный раствор иона Na+, являющегося общим ионом анионного красителя.
Активность красителя в растворе зависит, как известно, от температуры, концентрации и давления. Обычно величина сродства красителя к волокну выражается в джоулях на моль. Например, значение величины сродства различных прямых красителей к целлюлозе при температуре 100°С находится в пределах 13,4-22,7 кДж/моль.
|
| Величины сродства к коллагену различных кислотных красителей, кДж/моль (цифра около названия красителя означает степень его интенсивности) |
| |
25° С |
45° С |
| Оранжевый 7 |
44,5 |
45,7 |
|
| " 8 |
46,2 |
44,1 |
|
| Красный 13 |
69,3 |
73,9 |
|
| " 27 |
89,0 |
93,7 |
|
|
По величине сродства красителя к волокну при двух температурах можно рассчитать теплоту реакции красителя с волокном или теплоту крашения, которая является термодинамической величиной и наряду с величиной сродства характеризует процесс крашения. Она дает возможность описать количественно действие температуры на установление равновесия при крашении. Стандартную теплоту крашения ?Н° (энтальпию) можно рассчитать по формуле
|

|
Теплота крашения рассматривается как сумма тепловых эффектов, возникающих при крашении вследствие взаимодействия красителя с волокном, гидратации, дегидратации волокна и красителя, а также расклинивания макромолекул волокна при взаимодействии с красителем.
Экспериментально установлено, что теплота крашения хлопка прямыми красителями равна 54,2-69,3 кДж, коллагена кислотными красителями при температуре 25-45°С - 71,4-134,4 кДж. Т. Виккерстафф подчеркивает, что, по имеющимся данным, во всех случаях теплота крашения является величиной отрицательной, т. е. в процессе крашения тепло выделяется. Это означает, что при снижении температуры красильного раствора скорость крашения сильно замедляется (рис. 2).
|

Рис.2. Влияние температуры на скорость крашения и равновесие
(А,B,C,D -условное обозначение концентраций )
|
|
|













